Gut丨癌症关键基质细胞亚群及其驱动转移机制研究
癌症相关成纤维细胞(Cancer-associated fibroblasts,CAFs)是肿瘤微环境中最主要的基质细胞成分之一,在肿瘤发生、进展及转移过程中发挥关键调控作用。研究表明,CAFs可通过细胞外基质(ECM)重塑、分泌可溶性因子及外泌体,促进血管生成、免疫逃逸和代谢重编程,并通过与肿瘤细胞、免疫细胞及内皮细胞的复杂互作推动癌症恶性进展。然而,CAFs具有高度异质性,不同亚群在起源、表型和功能上存在显著差异。尽管已有少数研究从泛癌层面初步解析了CAFs的单细胞图谱,但针对关键亚群的功能特征及其分子调控机制仍缺乏系统性阐明。因此,鉴定泛癌保守的关键CAFs亚群并解析其功能与调控网络,对于全面揭示CAFs在肿瘤微环境中的功能角色具有重要意义,并有望为肿瘤治疗提供新的潜在干预靶点和策略。
近日,中山大学肿瘤防治中心研究员、中山大学香港高等研究院院长助理贝锦新和中山大学肿瘤防治中心副研究员罗春玲团队在国际权威期刊Gut上发表题为SDC1⁺ CAFs secreting CTGF drive tumour metastasis via FGFR3 signalling in cancers的研究论文。该研究整合了来自14种癌症类型的单细胞转录组数据,系统构建了泛癌CAFs的单细胞图谱。研究鉴定出一种在多种实体瘤中普遍存在、呈肿瘤特异性富集,并与淋巴结转移及患者不良预后显著相关的 SDC1⁺ CAFs 亚群。进一步结合体内外实验模型及分子机制研究,系统阐明了该亚群在肿瘤转移中的生物学功能及其作用机制,为实体瘤抗转移治疗提供了具有重要转化潜力的基质靶点。

研究团队整合了涵盖14种癌症类型、554例样本的单细胞转录组数据,构建了包含超过254万个细胞的泛癌单细胞图谱。通过无监督聚类分析共鉴定出31个CAF亚群,并进一步采用一致性评分算法筛选出5个在超过10种癌种中稳定存在的泛癌保守CAF亚群,其总量占肿瘤组织内CAFs比例的50%以上。其中,SDC1⁺ CAFs 为丰度最高的亚群,平均约占肿瘤组织内CAF总量的30%,而在癌旁组织中含量显著降低,呈现出明显的肿瘤特异性富集特征。临床相关性分析显示,SDC1⁺ CAFs 的丰度随肿瘤恶性进展及 TNM 分期升高而增加,并与淋巴结转移风险呈显著正相关,在转移灶中的比例高于原发灶组织。TCGA 生存分析进一步表明,该亚群高表达与患者总体生存期及疾病特异性生存期显著负相关。
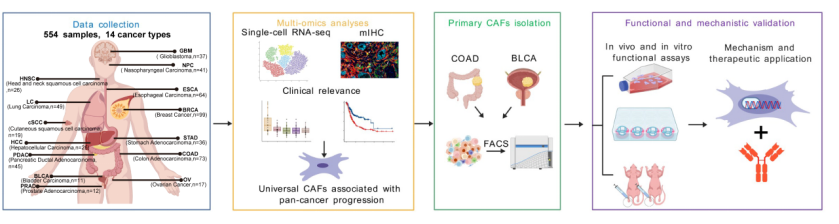
功能研究表明,SDC1⁺ CAFs 高表达ECM重塑及迁移调控相关基因,表现出更强的体外侵袭及基质重塑能力。在体外共培养体系中,SDC1⁺ CAFs 可诱导肿瘤细胞发生上皮–间质转化(EMT),并显著增强其迁移与侵袭能力;体内共接种瘤模型进一步证实,该亚群显著促进肿瘤细胞向淋巴结转移。机制研究显示,SDC1⁺ CAFs 高表达转录因子 KLF6,后者可直接结合 CTGF 启动子并激活其转录,促进 CTGF 表达。高表达的CTGF进而以旁分泌形式分泌到细胞外,激活肿瘤细胞表面 FGFR3 信号通路,驱动 EMT 进程并促进转移。过表达CTGF显著增强 SDC1⁻ CAFs 的促转移能力,而通过 siRNA 或中和抗体阻断 KLF6–CTGF–FGFR3 信号轴任一环节,均可显著逆转 SDC1⁺ CAFs 的促转移效应。临床病理分析进一步显示,KLF6 与 CTGF 表达水平呈显著正相关,且二者高表达均与患者不良预后密切相关,KLF6 与 CTGF 共同高表达患者的预后最差。
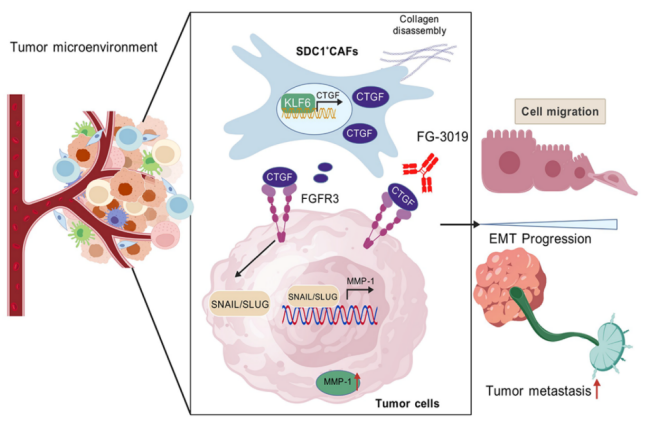
综上所述,该研究通过泛癌单细胞转录组整合分析,首次鉴定并系统验证了 SDC1⁺ CAFs 作为一种跨癌种保守存在的促转移CAF亚型,并全面阐明了其通过 KLF6–CTGF–FGFR3 信号轴驱动肿瘤细胞上皮–间质转化及转移的分子机制。该研究从泛癌层面揭示了CAF亚群在功能上的保守性及其在肿瘤转移过程中的关键调控作用,为深化对肿瘤微环境中基质细胞功能分化与生物学意义的理解提供了重要科学依据,并为实体瘤抗转移治疗策略的开发提出了兼具普适性与特异性的潜在基质靶点组合。

