科研成果

Gut丨癌症關鍵基質細胞亞群及其驅動轉移機制研究
癌症相關成纖維細胞(Cancer-associated fibroblasts,CAFs)是腫瘤微環境中最主要的基質細胞成分之一,在腫瘤發生、進展及轉移過程中發揮關鍵調控作用。研究表明,CAFs可通過細胞外基質(ECM)重塑、分泌可溶性因數及外泌體,促進血管生成、免疫逃逸和代謝重編程,並通過與腫瘤細胞、免疫細胞及內皮細胞的複雜互作推動癌症惡性進展。然而,CAFs具有高度異質性,不同亞群在起源、表型和功能上存在顯著差異。儘管已有少數研究從泛癌層面初步解析了CAFs的單細胞圖譜,但針對關鍵亞群的功能特徵及其分子調控機制仍缺乏系統性闡明。
STTT丨EB病毒劫持組蛋白去甲基化途徑促進上皮腫瘤惡性進展的新機制
EB病毒(Epstein-Barr virus, EBV)是首個被發現的人類腫瘤相關病毒,每年全球因EBV感染新發的腫瘤病例約20萬例。其中,源自上皮組織的惡性腫瘤——鼻咽癌(Nasopharyngeal carcinoma, NPC)和EBV相關胃癌(EBV-associated gastric cancer, EBVaGC)占比高達80%,嚴重威脅著人類的健康。儘管眾多研究已證明EBV與這些上皮惡性腫瘤的高度關聯,然而其驅動腫瘤發生和發展的致癌機制仍未被完全解析。
J Clin Invest丨貝錦新團隊揭示超級增強子驅動宮頸癌惡性進展的新機制
宮頸癌(Cervical cancer)作為全球女性第四大常見惡性腫瘤,其發病率和死亡率居高不下,嚴重威脅女性健康。宮頸癌發生發展涉及多種因素,包括高危型HPV亞型感染、個體的遺傳易感性及環境因素等。儘管早期患者可以通過手術和放化療獲得良好預後,但晚期或轉移性患者預後較差,5年生存率僅有16.5%。因此,深入研究驅動宮頸癌發生發展的致癌機制,探索新型診療靶點和診療策略,是提高宮頸癌患者療效的迫切需求,對於降低疾病負擔具有重要意義。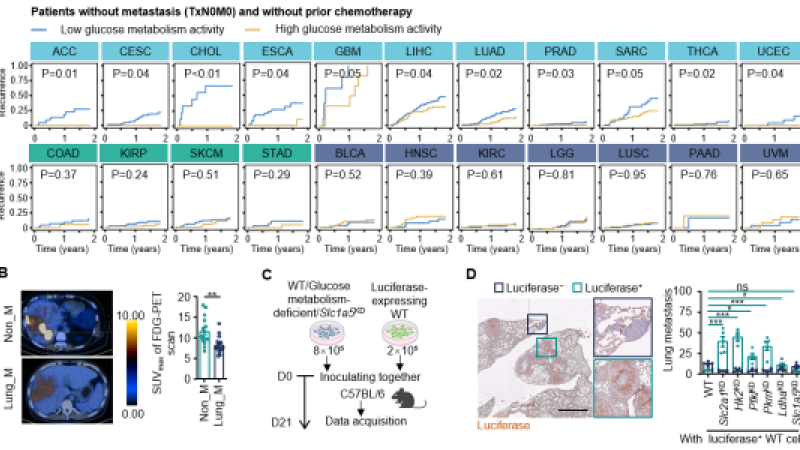
「控糖」促腫瘤轉移?葡萄糖限制誘導肺部促轉移免疫環境新機制
2025年7月15日,中山大學鄺棟明教授、魏瑗副教授團隊在《Cell》期刊發表題為《Glucose Restriction Shapes Pre-Metastatic Innate Immune Landscapes in Lung through Exosomal TRAIL》(影響因數:42.5)的研究論文。該研究通過大規模臨床數據、多組學分析與體內實驗,首次揭示葡萄糖剝奪可通過外泌體TRAIL重塑肺部免疫環境,誘導轉移前生態位形成的機制,並提出相應的干預策略。本研究由中山大學、中山大學香港高等研究院等單位合作完成。
《Cell》:多組織器官免疫細胞圖譜揭示系統免疫建立與耐受新機制
2025年10月28日,中山大学何晓顺、贝锦新、郭志勇、王子莲教授联合团队在Cell 杂志发表题为Systemic immune activity occurs during human immune system maturation的研究论文。该项研究基于胚胎及成人23种组织的321份样本,通过单细胞转录组及TCR测序技术,分析了超过280万个免疫细胞,首次系统性描绘了人类第二孕期免疫系统的动态发育图谱。

